ENFERMEDAD DE ALZHEIMER
Dilemas éticos emergentes ante los nuevos descubrimientos en el Alzheimer.
En
los últimos 50 años, el envejecimiento poblacional se ha incrementado,
aumentando dramáticamente el número de casos de patología cognitiva y demencia.
La
causa más frecuente de demencia degenerativa, tanto de inicio temprano (antes
de los 65 años) como de inicio tardío (luego de los 65 años) es la Enfermedad
de Alzheimer.
Los
nuevos criterios de Alzheimer, con la ayuda de biomarcadores, pueden
diagnosticar la enfermedad varios años antes de que el paciente ingrese al
estadio demencial (perdida de la funcionalidad)
La
ciencia ha tenido un notable avance en el conocimiento de la enfermedad y en el
diagnóstico temprano, pero no en la curación
de la misma.
Los
tratamientos actuales de la E. Alzheimer son sintomáticos y con una eficacia
pobre. Pocos son los estudios en la literatura que avalan que el tratamiento preventivo
(control de factores de riesgo vascular, actividad física aeróbica, dieta, etc)
retrase el deterioro. Por otro lado, las nuevas drogas antipatogénicas en
Alzheimer en estadíos más avanzados han mostrado resultados desalentadores.
Los
nuevos criterios de Alzheimer ponen al sujeto vulnerable
en la condición de “paciente
en espera” de la enfermedad, sin un tratamiento eficaz hasta el momento.
Pero por otro lado, la fase prodrómica del Alzheimer abre un enorme abanico de
posibilidades de investigación y un importante desafío clínico.
El
avance de la ciencia, enfrenta al médico (con nuestra idiosincrasia) a nuevos
dilemas: comunicar el diagnóstico de una enfermedad progresiva, irreversible,
altamente prevalente y hasta el momento incurable.
Estamos
los médicos preparados para enfrentar el dilema de comunicar esta enfermedad
antes de la demencia?
Al
revisar la literatura, nos encontramos que en los últimos años, ha
habido un cambio en la actitud sobre comunicar el
diagnóstico de una enfermedad al paciente, especialmente en el caso del cáncer.
La mayor parte de la literatura mundial en relación a comunicar el diagnóstico
está centrada en oncología (Pinner G, 2000). En 1961, se realizó un estudio que
mostró que el 90% de los médicos no revelaba el diagnóstico de cáncer a sus
pacientes, sin embargo, 20 años después el 98% de los médicos lo hacían,
implicando un cambio radical en la comunicación y el abordaje de este tipo de
enfermedades. Sin embargo, hay poca literatura sobre la comunicación diagnóstica
en demencias (Oken D, 1961; Novack D 1979). Las guías de la Asociación Médica
Americana (AMA) recomiendan dar el diagnóstico de Enfermedad de Alzheimer “si
es posible” (Raicher I, 2008; Johnson H, 2000). Las preguntas más
frecuentes que el médico se realiza a la hora de enfrentarse con un paciente
con Alzheimer prodrómico son doy el diagnóstico, a quién, al paciente o su
familiar previamente, cuando, cómo, para qué, se beneficiaría el paciente al
conocer su estado, tiene la capacidad para tomar decisiones acerca de su vida y
que tratamiento le ofrezco en consecuencia? Algunos estudios, reportan que el
40% de los especialistas comunica el diagnóstico de demencia a sus pacientes y
el 20% no ve ningún beneficio en hacerlo. El
principio ético mayormente involucrado en decir o no el
diagnóstico de Enfermedad de Alzheimer a un paciente es el de autonomía (Santander
F; 2000; Gómez-Lobo A 2006). El ejercicio de la autonomía de
las personas, exige que se cumplan al menos tres condiciones: actuar voluntariamente,
es decir, libre de coerciones, tener información suficiente sobre la decisión
que se va a tomar y tener capacidad, esto es, poseer una serie de aptitudes
psicológicas, cognitivas, volitivas y afectivas, que le
permitan conocer, valorar y gestionar adecuadamente la
información anterior, tomar una decisión y expresarla. El paciente tiene
derecho a saber su diagnostico, pero también a no saberlo si así lo desea, a
querer o no compartir el diagnostico con su familia y a planificar su vida de
la manera más apropiada según su enfoque. El paciente, para poder tomar estas
decisiones debe tener relativamente preservada su capacidad intelectual y es
precisamente el poder valorar la capacidad en este estadio tan temprano
de la enfermedad, una de las tareas más difíciles para el profesional. La
capacidad es
un atributo de las personas que tiene gran variabilidad. Una
persona puede ser capaz para una función pero
no para otra. Además puede variar en un mismo individuo a lo largo
del tiempo. (Simón P 2006). Las alteraciones neurológicas y cognitivas
influyen en la capacidad para decidir. Por eso, es de capital importancia una
exhaustiva evaluación neuropsicológica. Se considera que puntajes
menores a 19 en el test de Mini Mental (Folstein 1972) se asocian altamente con
incapacidad (Appelbaum P, 2007). Es importante destacar que un individuo que
preserva la conciencia de enfermedad o “insight” es capaz de verbalizar
la naturaleza, severidad y consecuencias de sus alteraciones cognitivas. Sin
embargo, los pacientes con gran conciencia de sus fallas cognitivas
suelen angustiarse más, como sucede en las personas que transitan la Enfermedad
de Alzheimer en etapa leve. El paciente con Enfermedad de Alzheimer en etapa
moderada y severa en general ha perdido la conciencia de enfermedad y se
encuentra por ende anosognósico y tal vez no se beneficie de la discusión
con él sobre su diagnóstico (Cornett P, 2008).
Los
trastornos afectivos juegan una gran influencia a la hora de valorar el peso que
le da el paciente a los riesgos y beneficios de un diagnostico o situación
determinada. Los pacientes depresivos, en general, tienden a hacer
valoraciones menos optimistas que los sujetos normales
en situaciones problemáticas. (Simón P, 2008).
Se
considera que la capacidad se pierde cuando un
individuo tiene una importante alteración la memoria de trabajo y sus
funciones ejecutivas, que son esenciales para la comprensión, toma de
decisiones y procesamiento cognitivo. (Cornett P, 2008).
Además
de la autonomía, está involucrado el principio ético de la no
maleficencia. La no maleficencia establece la obligación de no hacer el mal.
Al informar el diagnóstico de Enfermedad de Alzheimer al paciente, aunque ésta
sea la verdad, se puede hacer un daño por el impacto que esta noticia puede
tener sobre él. Esto se puede expresar en forma de depresión y en casos
extremos de ideación suicida (Paola Fuentes R, 2012).
Existen
varios estudios que reportan que los familiares piden al personal
de salud que no se le informe al paciente de su diagnóstico por miedo al
impacto psicológico que pueda tener. Algunos estudios revelan que el saber el
diagnóstico, podía ser un factor de reducción de ansiedad al tener una
explicación de los síntomas y proveer un plan de tratamiento y / o seguimiento
médico (Carpenter BD, 2008). Draper y colaboradores en 2010 reveló que al
informar el diagnostico al paciente, podría existir un riesgo de conducta
suicida (aunque mínimo), sobre todo en los tres
primeros meses del diagnóstico. Por este motivo. se recomienda
precaución en sujetos que tienen depresión
concomitante, cubriendo las necesidades emocionales del paciente posterior al diagnóstico
(Draper B 2010).
En
síntesis, el envejecimiento poblacional ha incrementado enfermedades
edad-dependientes como las demencias, siendo la Enfermedad de Alzheimer (EA) la
causa más frecuente en adultos mayores (50-60%). (Kukull WA 2000; Ferri
CP 2005). Es una de las enfermedades más temidas, por su carácter irreversible
e incurable, por su cronicidad y por consistir en un largo proceso de pérdidas
progresivas, aislando a la persona de su medio. Han surgido nuevos criterios
diagnósticos de EA basados en biomarcadores, los cuales se pueden realizar
en vida, anticipando el devenir de la demencia varios años antes (Dubois
B 2001; Dubois B 2010; Allegri RF 2012, Prvulovic D
2012). Por ende, los médicos se ven cada día más expuestos a pacientes con
EA en etapas más precoces, con plena conciencia de enfermedad,
debiendo enfrentar el dilema de comunicar el diagnostico, siguiendo los
lineamientos de la Ley de derechos del paciente, respetando la autonomía pero
sin que esto implique un daño peor que la propia dolencia. Los profesionales
médicos no reciben la capacitación adecuada acerca de cómo comunicar
diagnósticos de enfermedades incurables y son escasas las guías operativas
diagnosticas basadas en la ética de los nuevos avances científicos.
Los factores que contribuyen a generar dilemas de comunicación diagnostica ante
los nuevos avances de la ciencia son factores culturales, idiosincráticos, la
falta de conocimiento sobre el tema y la dificultad y complejidad en interpretar
los resultados de los nuevos biomarcadores, la falta de guías operacionales y
recomendaciones locales sobre el Alzheimer prodrómico y la escasa capacitación
en ética de los profesionales médicos que asisten pacientes con enfermedades
terminales.
Las
recomendaciones actuales de la Sociedad de Medicina Nuclear e Imágenes
Moleculares y la Asociación de Alzheimer (Journal of Nuclear
Medicine, published on January 28, 2013) sobre el uso apropiado e
inapropiado del PET con marcación de amiloide, se basan en situaciones médicas
determinadas, sin embargo, no han tenido en cuenta consideraciones
éticas a la hora de indicar estos estudios a los pacientes.
Ofrecer
el PET, sin previo consentimiento por parte del paciente, sin poder brindar
opciones de tratamiento y/ seguimiento, sin valorar el estado emocional actual
y previo, sin tener en cuenta la situación social, familiar o de red del
sujeto, serían usos inapropiados del PET, independientemente del diagnostico
clínico.
El
médico tendrá el importante rol de saber determinar caso por caso la decisión a
tomar en base a cada paciente en particular, respetando la autonomía y evitando
dañar a la hora de comunicar el diagnostico.
Dra
Cecilia Serrano
¿QUE ES ENFERMEDAD DE ALZHEIMER?
La enfermedad de Alzheimer es un trastorno
degenerativo e irreversible del cerebro que causa un deterioro progresivo de la
capacidad intelectual, comenzando en general por pérdida de memoria, problemas
del lenguaje y desorientación en tiempo y espacio.
Su nombre proviene de Aloís Alzheimer, un neurólogo
alemán que en 1906 quien describió los síntomas que presentaba una mujer de 48
años como “graves problemas de memoria y de conducta” así como las
características neuropatológicas de la enfermedad de Alzheimer. La enfermedad
suele tener una duración media aproximada después del diagnóstico de 10 años,
aunque esto puede variar en proporción directa con la severidad de la
enfermedad al momento del diagnóstico
La enfermedad de Alzheimer es la forma más común de
demencia, es incurable y terminal, que aparece con mayor frecuencia en personas
mayores de 65 años de edad.
Cuáles son los síntomas?
Por lo general, el síntoma inicial es la dificultad
para adquirir nueva información y por ende memorizarla. Los pacientes se
olvidan de lo reciente, suelen repetir las cosas, a veces faltan las palabras,
confunden los nombres al hablar, pueden desorientarse en lugares conocidos y no
saber exactamente la fecha, el mes o el año. Los síntomas son progresivos y van
llamando la atención al entorno familiar. Al principio, suele confundirse con
actitudes relacionadas con la vejez o con el estrés.
A medida que progresa la enfermedad, aparecen
confusión mental, irritabilidad y agresión, cambios del humor, trastornos del
lenguaje, pérdida de la memoria de largo plazo y una predisposición a aislarse
a medida que los sentidos del paciente declinan.
El pronóstico es difícil de determinar. Se estima que
el promedio general es de 7 años, menos del 3% de los pacientes viven por más
de 14 años después del diagnóstico.
Cuál es la causa?
La causa del alzhéimer permanece desconocida. Las
investigaciones suelen asociar la enfermedad a la aparición de placas seniles y ovillos
neurofibrilares.
Como se trata?
Existen tratamientos farmacológicos (donepecilo,
galantamina, rivastigmina y memantine) y no farmacológicos (estimulación cognitiva,
actividad física aeróbica) y psi coeducación a la familia para el manejo del
paciente y para evitar la sobrecarga que lleva a la depresión, ansiedad y
enfermedad del familiar que asiste diariamente al enfermo.
Los tratamientos actuales ofrecen moderados beneficios
sintomáticos. No hay tratamiento que cure la enfermedad. Para la
prevención del alzhéimer, se propone modificar hábitos de alimentación,
realizar actividad física, disminuir los niveles de colesterol, controlar los
factores de riesgo de riesgo vascular.
Que debe
hacerse?
Ante la sospecha de Alzhéimer, se debe concurrir al
médico de cabecera, quien podrá pedir la derivación al especialista en
patologías cognitivas.
El diagnóstico se realiza con evaluación
neuropsicológica y neuropsiquiátrica, así como neuroimágenes (Tomografía
cerebral o Resonancia magnética) y análisis de sangre para descartar problemas
tiroideos, déficits de vitaminas B12, acido fólico o infecciones como la
neurosifilis (VDRL), entre otros.
El Día Internacional del
Alzhéimer se celebra el 21 de setiembre, fecha elegida por la OMS y
la Federación Internacional de Alzhéimer, en la cual se celebran en
diversos países actividades para concientizar y ayudar a prevenir la
enfermedad.
BIBLIOTECA VIRTUAL:
Revisión de los últimos artículos científicos destacados acerca de la enfermedad de ALZHEIMER.
Ethical
issues in Alzheimer's disease: an overview.
McGill Centre for Studies in Aging, Douglas Mental Health University
Institute, Montreal, QC, Canada. antoine.leuzy@mail.mcgill.ca
Expert Rev Neurother. 2012 May;12(5):557-67. .
La enfermedad de
Alzheimer (EA) es responsable de la
mayoría de los casos de demencia. Los médicos, pacientes, familiares, cuidadores y los
investigadores se enfrentan a numerosos
problemas éticos que varían y evolucionan en función del estadio de la enfermedad y su gravedad.
Revelar un diagnóstico de demencia
tipo Alzheimer es bastante difícil.Los
avances en la neurobiología de la misma han llevado a un creciente cambio en el diagnóstico,
realizándose en sus fases pre-demencia , cuando
los pacientes tienen una visión completa de su pronóstico. Los problemas genéticos en el Alzheimer
son de gran importancia, en el caso de familias con formas de inicio precoz (antes de los 65), debido a la presencia de mutaciones determinantes. La
prueba genética para la apolipoproteína
E (APOE) - un factor de riesgo para la EA esporádica
- es ampliamente debatido, puede ser necesaria en el contexto de nuevos medicamentos modificadores de la enfermedad. Los medicamentos sintomáticos actuales - inhibidores
de la colinesterasa (IC) y el
NMDA antagonista del receptor de memantina - son
relativamente fáciles de usar, aunque con eficacia
limitada, pero su acceso es restringido
en muchos países por
consideraciones económicas. Al final de la vida la
atención se está moviendo lentamente hacia un enfoque de atención paliativa similar a la del cáncer en fase terminal. Habrá nuevos medicamentos en el futuro cercano, algunos de los que
retrasarán la progresión de
estadios prodrómicos a la demencia, pero su uso requiere cuidadosas reglas de control.
Minn Med. 2012 Jan;95(1):42-5.
New
clinical criteria for the Alzheimer's disease spectrum.
Mayo Alzheimer's
Disease Research Center, USA.
Se han publicado recientemente Nuevos criterios para el
diagnóstico de la enfermedad de Alzheimer (EA). Estos criterios abarcan todo el
espectro de la EA como la demencia de Alzheimer, el deterioro cognitivo leve
debido a EA y EA preclínica. Una característica importante de los nuevos
criterios es que distinguen entre las características clínicas de la enfermedad
y las características patológicas. Los criterios anteriores se basaron en las
características clínicas. Los nuevos criterios incluyen el uso de imágenes y
de biomarcadores para ayudar en el
diagnóstico. Los criterios relacionados a las características clínicas se están
utilizando actualmente en la práctica diaria. Muchos autores, entre ellos
Ronald Petersen, consideran que los
criterios sobre los biomarcadores aún deben ser validados. A continuación se expondrán los artículos mencionados.
Evolution of the diagnostic criteria for degenerative and cognitive disorders from Dario Yac
Cholesterol and Statins in Alzheimer’s Disease:II. Review of Human Trials and Recommendations
Cholesterol and Statins in Alzheimer’s Disease:II. Review of Human Trials and Recommendations
Nina E. Shepardson, M.S.1, Ganesh M. Shankar, M.D., PhD.1,2, and Dennis
J. Selkoe, M.D.1,*
Hay mucha evidencia en
el último tiempo sobre la hipótesis de que los niveles elevados de colesterol pueden
aumentar el riesgo de desarrollar enfermedad de Alzheimer (EA).
Si bien, los resultados
de varios estudios con estatinas han avalado su uso en EA, sin embargo, cuando
se revisa la literatura en humanos, los
resultados son muy variables, lo que hace difícil
sacar conclusiones firmes. Este artículo identifica varios factores de confusión entre los estudios en humanos, formulando recomendaciones para los futuros estudios, entre ellos, tener en cuenta las diferentes permeabilidades de la barrera hematoencefalica de las estatinas a la hora de analizar los resultados y realizar ensayos con estatinas en el tratamiento en pacientes con EA leve, que tienen las mejores posibilidades de modificación de la enfermedad.
sacar conclusiones firmes. Este artículo identifica varios factores de confusión entre los estudios en humanos, formulando recomendaciones para los futuros estudios, entre ellos, tener en cuenta las diferentes permeabilidades de la barrera hematoencefalica de las estatinas a la hora de analizar los resultados y realizar ensayos con estatinas en el tratamiento en pacientes con EA leve, que tienen las mejores posibilidades de modificación de la enfermedad.
Vertex. 2012
Jan-Feb;23(101):5-15.
Review of recommendations and new diagnosis
criteria for mild cognitive impairment due to Alzheimer's disease]
Allegri RF,
Russo MJ,
Kremer J,
Taragano FE,
Brusco I,
Ollari JA,
Serrano CM,
Sarasola D,
Demey I,
Arizaga RL,
Bagnati P.
La fase predemencia
de la enfermedad de Alzheimer (EA), conocida como deterioro cognitivo leve
(DCL) es una condición clínica y neuropsicológica que define el estado de
transición entre el envejecimiento normal y la demencia, y se utiliza como una
descripción clínica de las personas en riesgo de desarrollar EA. Esta es una
revisión de los criterios diagnósticos publicados recientemente por la
Asociación de Alzheimer y el Instituto Nacional del Envejecimiento de los
EE.UU. con el fin de garantizar el diagnóstico precoz de la enfermedad, útil
para la práctica clínica y para los ensayos clínicos. Los
objetivos de este trabajo son analizar los criterios revisados para el diagnóstico de MCI debido a la enfermedad de Alzheimer recientemente propuestos, al comparar con los
criterios de MCI disponibles.
Los
nuevos criterios para el diagnóstico de MCI debido a EA tienen una gran importancia.
Ellos
proporcionan una herramienta útil, coherente y valiosa para homogeneizar el subgrupo de pacientes con deterioro cognitivo leve que ya tiene
Alzheimer en una fase predemencia.
Genetic counseling and testing for Alzheimer disease: Joint practice guidelines of the American College of Medical Genetics and the National Society of Genetic Counselors
Jill S.
Goldman, MS, MPhil,1,2 Susan E. Hahn,
MS,3 Jennifer
Williamson Catania, MS, MPH,1,2 Susan
LaRusse-Eckert, MS,2 Melissa
Barber Butson, ScM,4 Malia
Rumbaugh, MS,5 Michelle N.
Strecker, MS,6,7 J. Scott Roberts,
PhD,8 Wylie Burke,
MD, PhD,9 Richard
Mayeux, MD, MSc,1,2 and Thomas Bird,
MD10
La enfermedad de
Alzheimer es la causa más común de demencia.
Ocurre en todo el mundo
y afecta a todos los grupos étnicos. La
incidencia de la enfermedad de Alzheimer está aumentando debido, en parte, a la
mayor esperanza de vida y el envejecimiento poblacional. El
riesgo promedio de desarrollar la enfermedad de Alzheimer es de 10-12%. Este
riesgo se duplica por lo menos con la presencia de un familiar de primer grado
con la enfermedad. A
pesar de su utilidad limitada, los pacientes expresan su preocupación por el
riesgo y, en algunos casos, solicitan cada vez más pruebas genéticas.
Sin
embargo, debido a la complicada naturaleza genética del trastorno, pocos son
los profesionales que están preparados para abordar los riesgos genéticos de la
enfermedad de Alzheimer con sus pacientes.
Esta
guía práctica ofrece a los médicos un marco para evaluar el riesgo genético de
sus pacientes con enfermedad de
Alzheimer o de sus familiares, para identificar a los individuos que pueden
beneficiarse de las pruebas genéticas y para disponer de los elementos claves de la
asesoría genética para la EA.
Trials. 2012 Jul 2;13:98. doi: 10.1186/1745-6215-13-98.
A benefit-finding intervention for family caregivers of persons with Alzheimer disease: study protocol of a randomized controlled trial.
Los cuidadores de familiares con enfermedad de Alzheimer suelen
estar muy estresados y en riesgo de desarrollar enfermedades físicas y psiquiátricas. Este
trabajo revela el beneficio de las intervenciones en los familiares. Las
intervenciones suelen centrarse en proporcionar a los cuidadores psi coeducación: conocer la demencia, disponer
de diferentes estrategias y/o habilidades
y brindar el apoyo para ayudar a lidiar el estrés asociado a su cuidado.
Rocz Panstw Zakl Hig. 2012;63(2):135-40.
[Nutritional factors in prevention of Alzheimer's disease].
El hábito nutricional
afecta significativamente el cuerpo del hombre en cada época.
Los adultos mayores a
menudo requieren intervenciones dietéticas específicas.
Una dieta adecuada y
equilibrada es un elemento importante del estilo de vida que puede convertirse
en un factor que facilita el llamado envejecimiento saludable, exitoso y pueda retrasar
el desarrollo de enfermedades crónicas no infecciosas /o metabólicas que son en
la mayoría de los casos diagnosticados en personas mayores.
Las enfermedades
neurodegenerativas se han clasificado entre las enfermedades crónicas de
etiología aún no determinada. Sin
embargo, se especula que algunos factores nutricionales, incluyendo la ingesta
adecuada de vitaminas del grupo B, vitaminas antioxidantes y ácidos grasos
poliinsaturados, es probable que desempeñen un papel importante en la
prevención y la terapia. Una
dieta rica en vegetales y frutas, pan, leche y los productos lácteos, así como los que
contengan pescado, aceites vegetales y frutos secos proporciona todos los
nutrientes indispensables. La
adecuada combinación de estos alimentos en los platos - ampliamente descrito en
la literatura como la dieta mediterránea
facilita llevar una vida más saludable y
duradera.
Nutr
J. 2011 Sep
26;10:98. doi: 10.1186/1475-2891-10-98.
A prospective study of nutrition education and oral nutritional supplementation in patients with Alzheimer's disease.
La pérdida de peso en pacientes con enfermedad de Alzheimer
(EA) es una manifestación clínica común que puede tener importancia clínica. Los
objetivos de este artículo son evaluar si existe una diferencia entre la
educación nutricional y la suplementación nutricional oral sobre el estado
nutricional en pacientes con EA.
Métodos: Un estudio aleatorizado, prospectivo de 6 meses de
duración en el que participaron 90 sujetos con EA probable de 65 años o mayores
divididos en 3 grupos: grupo control (GC) [n = 27], Education Group (EG) [n =
25], que participó en un
grupo del programa de educación y suplementación (SG) [n = 26], que recibió dos
porciones diarias de suplementos nutricionales. Los
sujetos fueron evaluados para los datos antropométricos (peso, talla, IMC, TSF,
AC y AMC), datos bioquímicos (proteínas totales, albúmina y recuento total de
linfocitos), CDR (Clinical Dementia Rating), MMSE (Mini-Mental State
Examination), así como
la dependencia de las comidas.
RESULTADOS: La SG mostró una mejora significativa
en las medidas antropométricas siguientes: peso (H calc = 22,12, p =
<0,001), IMC (H calc = 22,12, p = <0,001), AC (H calc = 12,99, p =
<0,002) , y
AMC (H calc = 8,67, p = <0,013) en comparación con el CG y EG.
CONCLUSIÓN: La Suplementación nutricional oral
es más eficaz en comparación con la educación nutricional en la mejora del
estado nutricional de los pacientes con EA.
IMC de la EG fue significativamente mayor en comparación con
el CG. No
hubo cambios significativos en la proteína total (H calc = 6,17, p =
<0,046), y el recuento total de linfocitos en la SG en comparación con los
otros grupos (H cal = 7,94, p = 0,019).
Arch
Neurol. 2011
Jun;68(6):743-52. doi: 10.1001/archneurol.2011.125.
Diet intervention and cerebrospinal fluid biomarkers in amnestic mild cognitive impairment.
Bayer-Carter JL, Green PS, Montine TJ, VanFossen B, Baker LD, Watson GS, Bonner LM, Callaghan M, Leverenz JB, Walter BK, Tsai E, Plymate SR, Postupna N, Wilkinson CW, Zhang J, Lampe J, Kahn SE, Craft S.
Cuarenta y nueve adultos mayores (20 adultos sanos con una
media de edad de 69,3 [7,4] años y 29 adultos con Deterioro cognitivo leve
amnésico DCLa con una edad media de 67,6 [6,8] años).
INTERVENCIÓN: Los participantes recibieron una
dieta rica en calorías (grasa, 45%
[grasas saturadas,> 25%]; hidratos de carbono, 35% -40% [índice glucémico,>
70], y proteína, 15% -20%) o una dieta
reducida en calorías (grasa, 25%;
[grasas saturadas, <7%]; hidratos de carbono, 55% -60% [índice glucémico,
<55], y proteína, 15% -20%) durante 4 semanas.
Se realizaron pruebas cognitivas, pruebas de tolerancia oral
a la glucosa, punción lumbar al inicio del estudio y durante la cuarta semana
de la dieta. La principales medidas de resultado fueron: Las concentraciones en
el LCR de β-amiloide (Aß42 y Aβ40), proteína tau, insulina, F2 isoprostanos-, y
apolipoproteína E, lípidos
e insulina en plasma, y medidas de cognición.
RESULTADOS: Para el grupo DCLa, la dieta reducida en calorías: en LCR
aumentó las concentraciones de Aß42, en contra del patrón patológico de baja
CSF Aß42 típicamente observado en la enfermedad de Alzheimer. La
dieta baja en calorías tuvo el efecto opuesto en los adultos sanos, es decir,
la disminución de Aß42 CSF, mientras que la dieta hipercalórica aumentó CSF
Aß42. La
concentración de apolipoproteína E CSF aumentó en la dieta baja y disminuyó la
dieta alta en ambos grupos. Para
el grupo de MCIa, la concentración de
insulina aumentó con la dieta reducida.
La
dieta calórica aumentó los niveles de lípidos en plasma y la dieta reducida en
calorías los disminuyó. Mejoró la
memoria en después de la finalización de las 4 semanas de la dieta reducida en
calorías.
CONCLUSIÓN: Los resultados sugieren que la
dieta puede ser un poderoso factor ambiental que modula el riesgo de Alzheimer a
través de sus efectos sobre las concentraciones centrales de de Aß42 en el sistema
nervioso, lipoproteínas, del estrés oxidativo y de la insulina.
Proteínas
malformadas pueden ser clave en el diagnóstico temprano de la enfermedad de
Alzheimer
Un estudio ha revelado la eficacia de una
nueva técnica para localizar unos fragmentos proteicos que podrían ser claves
en el diagnóstico de la enfermedad de Alzheimer (EA). Los autores indican que
el nuevo método puede suponer una mejora en la valoración de la EA, que ahora
se detecta en etapas muy avanzadas principalmente a través del examen clínico,
técnicas de neuroimagen y análisis del líquido cefalorraquídeo.
El estudio se basa en la detección de los
oligómeros Aβ que son los precursores de las placas amiloides típicas de la EA,
estructuras que se considerada que producen el daño neuronal en el cerebro de
los pacientes. Se trata de una tecnología denominada PMCA (protein misfolding cyclic
amplification), que detecta la presencia de proteínas malformadas
características de este tipo de patologías.
El uso de este método en pacientes con EA
mostró una alta eficacia para localizar los oligómeros Aβ en concentraciones
muy bajas y, según los autores, fueron capaces de discernir entre pacientes con
EA o con otras patologías neurodegenerativas con un bajo porcentaje de error.
El siguiente paso en la investigación
consistiría en adaptar el uso de esta tecnología en muestras de sangre y orina
para conseguir un método mucho menos invasivo.
Les dejo el link:
---------------------------------------------------------------------
Afasia Progresiva Primaria: Evaluación de 26 casos.
Dra. Cecilia M. Serrano
La Afasia Progresiva Primaria (APP) fue
descripta originalmente por Mesulam en 1982; constituye una
entidad sindromática focal de evolución lenta hacia la demencia, secundaria a etiología
degenerativa con gran diversidad en la anatomía patológica. Se reconocen tres
variantes: afasia no fluente (APP NF), afasia fluente (APP F) y afasia
logopenica (APP L). En la revista Neurology del 2011 se han publicado
nuevos criterios para la clasificación de la Afasia Progresiva Primaria,
estableciendo criterios diagnósticos para estas tres variantes, con un
exhaustivo análisis de sus características clínicas. Se perfilan tres tipos de
diagnóstico para cada una: diagnóstico clínico, diagnóstico con apoyo de
neuroimagen y diagnóstico con patología definida (cambios anatomopatológicos o
mutaciones genéticas asociadas con el espectro de la degeneración
frontotemporal, la Enfermedad de Alzheimer u otra enfermedad específica). A
pesar de afectar el principalmente el lenguaje, se han descripto trastornos cognitivos
y neuropsiquiátricos asociados.
El Objetivo
del trabajo es describir
las características cognitivas, lingüísticas, neuropsiquiatrías y clínicas de
la APP.
PACIENTES Fueron
estudiados 26 pacientes con APP (Mesulam, 2001) y 20 controles normales
apareados por edad y escolaridad. Los pacientes con APP fueron clasificados por
tipo de APP: 3 variantes: Afasia no fluente, afasia fluente y logopénica
progresiva.(Gorno-Tempini y cols. 2004)
y por tipo de afasia.
INSTRUMENTOS UTILIZADOS
Cognitivo:
Mini Mental State Examination (Folstein, 1975)
Batería Neuropsicológica completa
Evaluación del lenguaje
Conductual:
Neuropsychiatric Inventory (NPI-Q Kauffer y
cols 2000)
Inventario
de depresión de Beck
Estadio de demencia:
Clinical Dementia Rating - (Huges,1982)
Tabla 1:
Datos demográficos
Resultados
- 46% APP no fluente: 12 casos (10 AB, 1 ATM, 1 mutismo aquinético)
- 31% APP fluente: 8 casos (4 ATS, 4 AW)
- 23% APP logopénica: 6 casos (6 AA)
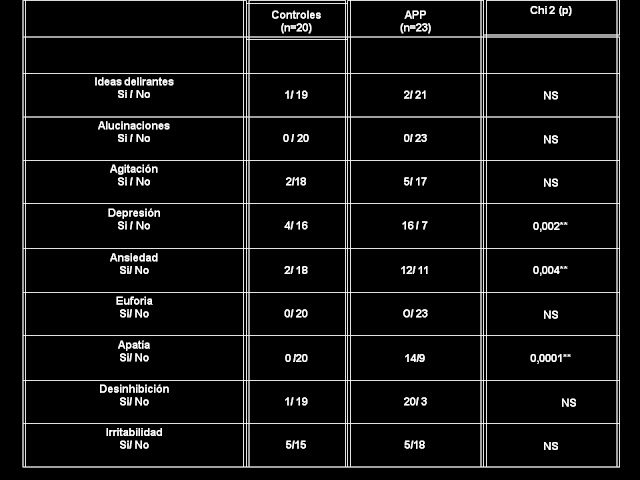
Tabla 2: Datos Neuropsiquiátricos de controles y
pacientes con APP
Ref: los valores de edad, escolaridad, MMSE, NPI y de Beck
total están expresados en media y desvío estándar. El sexo está expresado en
número de sujetos.‡ (p < 0.05)
Presencia de síntomas psiquiátricos
* *
Diferencias significativas entre grupos de controles y APP (p <
0.005).
Examen físico
39% evaluación
neurológica normal: 10 pacientes
27% anomalías en
los ROT: 7 pacientes
20% signos
arcaicos: 5 pacientes
20% signos
extrapiramidales: 5 pacientes
8% trastornos oculomotores:
2 pacientes
4% signos de compromiso de neurona motora: 1
caso
Evaluación Neuropsicológica:
54% dificultades ejecutivas
38% valores descendidos en test de memoria
verbal
19% evaluación cognitiva normal
19% no pudo ser evaluado por los
severos trastornos linguísticos
Neuroimágenes en APP
Afasia trans sensorial
Afasia anómica
Conclusiones
- Entidad poco frecuente con presentación Heterogénea (lenguaje, neuropsiquiatría, manifestaciones neurologicas y anatomopatologicas).
- prevalencia de APP no fluentes con respecto a las fluentes.
- A pesar de la escasa queja psiquiátrica, los trastornos de conducta fueron mas prevalentes de lo esperado, cuando fueron evaluados con escalas especificas (NPI y Beck).
- El único denominador común a todas ellas, es la predilección anatómica por las áreas del lenguaje en el hemisferio dominante.








2 comentarios:
Sería ingrata si decidiera no compartir nuestra experiencia de éxito con ZOMO, nací como cuidadora, por lo que me resulta difícil ver mis propias necesidades por separado de las necesidades de mi papá. La mayoría de los pacientes solo necesitan que alguien los abrace y les diga que no valen la pena, el tratamiento que probé no solo funcionó, sino que creo que lo curó.
Fue diagnosticado en 2011. Llevé a papá al médico de cabecera después de notar que se había vuelto cada vez más olvidadizo y vago. La clara señal de que algo estaba mal vino cuando condujo su auto a las tiendas locales (a cinco minutos en auto), compró sus compras, luego caminó de regreso a casa, olvidando que el automóvil estaba estacionado afuera de la tienda. Al día siguiente me llamó para decirme que me habían robado el coche. No tenía ningún recuerdo de dejarlo atrás. Después de una semana comenzó a repetirse y hacer las mismas preguntas. Lucharía por recordar conversaciones que solo habían ocurrido cinco minutos antes.
Su situación era muy complicada. Entiendo cómo se siente una hija y una vez cuidadora, la pérdida de memoria es mucho más complicada. Muchos se han visto condicionados a pensar que la medicina tradicional no ha encontrado una cura para una enfermedad. ZOMO ha desafiado este tren de mi pensamiento. Cuando estaba enfermo, fue una tragedia, lo soporté, me quebranté, supe dificultades, me perdí. Pero aquí estoy y puedo decirte inequívocamente que mi papá está curado. Esos de nosotros que hemos sido quebrantados entendemos el significado de la pérdida de memoria. Cuando miro el pasado y empiezo a escribir esto, las lágrimas de alegría me abruman. Me doy cuenta de que cada vez que pensaba que me rechazaban por algo bueno, en realidad me estaban redirigiendo a algo mejor. Fue uno de mis trabajos más difíciles y en el que vertí mi corazón y mi alma diariamente. Teniendo en cuenta lo bien que mi papá progresó en ese espacio de tiempo y ahora. No hay más síntomas de pérdida de memoria por más de 6 meses ahora. La cosa es que me da paz cuando papá está bien cuidado: cuando está feliz, yo estoy feliz. En este momento, todo se trata de él ... Siempre entro en su mundo para que podamos manejar la vida juntos. Nos levantamos cada mañana con una sonrisa y esperamos con ansias lo que nos traerá el nuevo día. Póngase en contacto con él en charantova@gmail.com
CÓMO ME CURÉ DE LA ENFERMEDAD DE ALZIEMEIR
Me diagnosticaron (enfermedad de Alzheimer) durante los últimos 2 años, lo que me hizo perder mi trabajo y mi relación con mi prometido después de que él descubrió que tenía la enfermedad de Alzheimer, ella me dejó e hice todo lo posible para que se quedara, pero ella Me descuidó hasta que un amigo mío del Reino Unido me dijo que era un gran curandero, que me devolverá la vida con su poderosa medicina curativa a base de hierbas. Luego me envió su dirección de correo electrónico para contactarlo- drimolaherbalmademedicine@gmail.com. Y lo contacté rápidamente, y me dijo que mi condición se resolverá en unas semanas, que tratará la enfermedad de inmediato solo si puedo aceptar la confianza en él y aceptar sus términos y condiciones. Estoy de acuerdo porque necesitaba ayuda. por supuesto, así que hice todo lo que me ordenó. Y sorprendentemente después de dos semanas, me envió un mensaje de texto, que debía apurarme al hospital para un chequeo, lo cual realmente hice, confirmo por parte de mi médico que ahora soy (Alziemeir Negative) mi corazón se llenó de alegría, porque realmente la enfermedad me privó de muchas cosas de mi vida, esto es un milagro, el dr imoloa también usa su poderosa medicina herbal para curar las siguientes enfermedades: enfermedad de lupus, úlcera bucal, cáncer de boca, dolor corporal, fiebre, hepatitis ABC, sífilis, diarrea , VIH / SIDA, enfermedad de Huntington, acné de espalda, insuficiencia renal crónica, enfermedad de Addison, dolor crónico, enfermedad de Crohn, fibrosis quística, fibromialgia, enfermedad inflamatoria intestinal, enfermedad micótica de las uñas, enfermedad de Lyme, enfermedad de Celia, linfoma, depresión mayor, melanoma maligno , Manía, melorreostosis, enfermedad de Meniere, mucopolisacaridosis, esclerosis múltiple, distrofia muscular, artritis reumatoide, enfermedad de Alzheimer, enfermedad de parkison, cáncer de vagina, epilepsia, trastornos de ansiedad, enfermedad autoinmune, dolor de espalda, dolor de espalda ain, trastorno bipolar, tumor cerebral, maligno, bruxismo, bulimia, enfermedad del disco cervical, enfermedad cardiovascular, neoplasias, enfermedad respiratoria crónica, trastorno mental y del comportamiento, fibrosis quística, hipertensión, diabetes, asma, artritis inflamatoria mediada por autoinmunidad. Enfermedad renal crónica, enfermedad inflamatoria de las articulaciones, impotencia, espectro del alcohol feta, trastorno distímico, eccema, tuberculosis, síndrome de fatiga crónica, estreñimiento, enfermedad inflamatoria intestinal, cáncer de huesos, cáncer de pulmón. contáctelo en el correo electrónico- drimolaherbalmademedicine@gmail.com. Y también en whatssap- +2347081986098. / Sitio web: http / www.drimolaherbalmademedicine.wordpress.com
Publicar un comentario